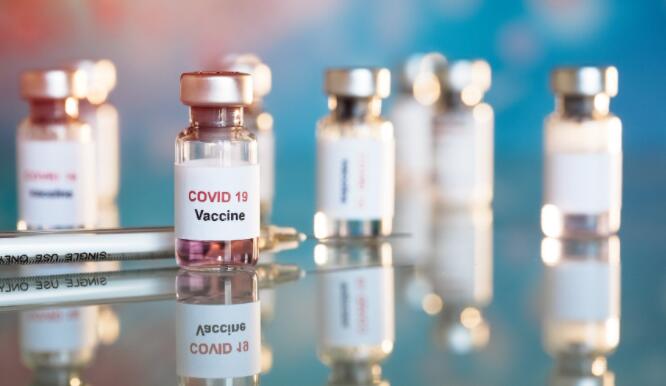
FDA咨询委员会推荐辉瑞局势疫苗的紧急授权
来源:
一个咨询委员会,美国食品和药物管理局(FDA)晚投票周四建议紧急使用授权(EUA)给予辉瑞公司的(NYSE:PFE)和BioNTech的(NASDAQ:BNTX)当前局势疫苗BNT162b2。FDA不必遵循委员会的建议,但是在加拿大和英国都批准紧急使用该疫苗之后,FDA会普遍这样做。
疫苗和相关生物制品咨询委员会(VRBPAC)由独立的行业疫苗专家组成。委员会成员在星期四花了几个小时讨论辉瑞和BioNTech的BNT162b2 EUA申请。该委员会特别关注疫苗的安全性。
最终,所有这些都归结为一个向VRBPAC委员会成员提出的问题。他们被问到:“基于现有的全部科学证据,辉瑞-BioNTech 当前局势疫苗的益处是否超过了其在16岁及16岁以上人群中使用的风险?”委员会以17票对4票赞成,弃权,认为该问题的答案是“是”。
赞成票不足为奇。FDA在本周早些时候向咨询委员会发布了简报文件,以审查其似乎赞成BNT162b2的功效和安全性。这些文件显示,辉瑞和BioNTech的疫苗在首剂后达到52.4%的功效。
现在,球在FDA法庭上。卫生与公共服务部部长亚历克斯·阿扎尔(Alex Azar)公开表示,该机构将在咨询委员会的建议后“几天内”做出决定。世界正在调整。
郑重声明:本文版权归原作者所有,转载文章仅为传播更多信息之目的,如有侵权行为,请第一时间联系我们修改或删除,多谢。